Б Пояснения
(0) Перфузия изолированных органов. Научная справка / (1) В начале обычно отказывает тело. Лечение болезней пересадкой головы / (2) Да и рак мозга (первичный или вторичный) легче лечить при изоляции мозга от тела / (3) Невозможность создания медицинской услуги значительно (за видовой предел) увеличивающих продолжительность жизни / (4) Внедрения перфузионных систем в медицину / (5) Сделать органы для пересадки бессмертными / (6) Аутотрансплантацию органов после восстановления / (7) Метод цифрового двойника / (8) Центры биоинженерной реконструкции органов / (9) Перфузия изолированной печени (причины выбора на первом этапе) /
(0) Перфузия изолированных органов. Научная справка.
«EVMP ex vivo (машинная перфузия)был создан в качестве альтернативы стандарту лечения статическим холодом, позволяющему длительно сохранять и контролировать качество органов в режиме реального времени, одновременно уменьшая/предотвращая ишемически-реперфузионное повреждение. Более того, это открыло путь к привлечению доноров с расширенными критериями, например, после сердечно-сосудистой смерти, тем самым расширив пул донорских органов. Постоянное совершенствование протоколов EVMP, особенно увеличение продолжительности хранения, проложило путь к его более широкому применению, в частности, для восстановления и модификации больных органов, а также для лечения опухолей и инфекций и регенеративных подходов. Более того, внедрение EVMP для доклинических исследований in vivo , улучшающих моделирование заболеваний, вызывает значительный интерес, обеспечивая при этом идеальный интерфейс для биоинженерии и генетических манипуляций. Эти подходы могут применяться не только при аллогенной и ксеногенной трансплантации, но и при аутологичной трансплантации, когда пациенты могут находиться на временной органной поддержке, в то время как больные органы лечатся ex vivo с последующей реимплантацией вылеченного органа.» [*]
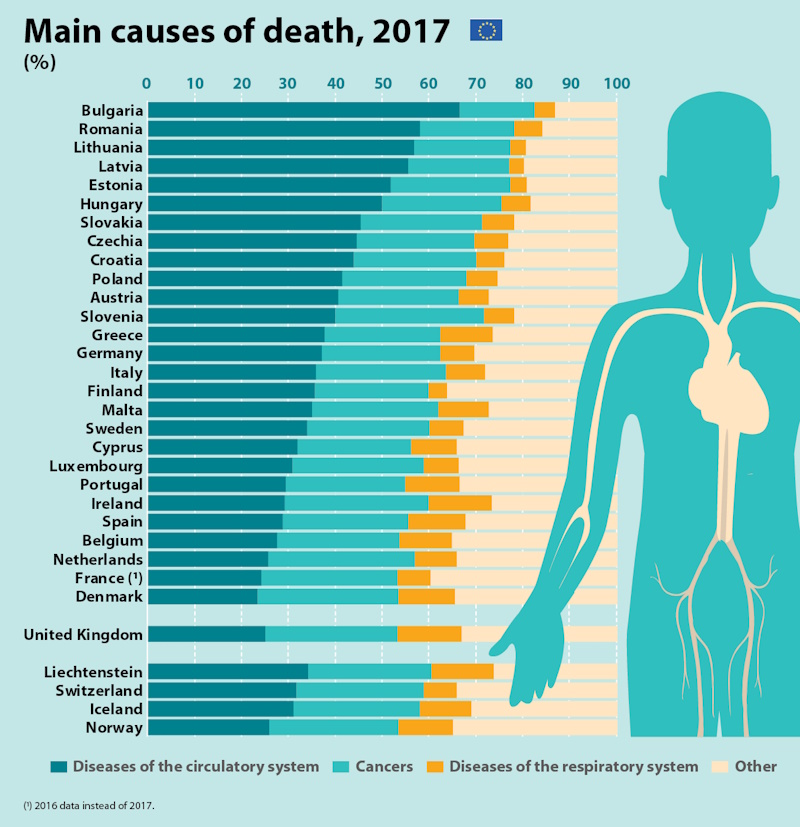
(1) В начале обычно отказывает тело. Так в государствах-членах ЕС болезни системы кровообращения и онкологические заболевания в совокупности составили более половины причин смерти, варьируясь от 52% во Франции (данные 2016 года) до 82% в Болгарии. После этих двух заболеваний третьей основной причиной смерти в большинстве государств-членов ЕС были заболевания дыхательной системы.
В работе за 1991 год указано, что общая распространенность деменции в Европе для пятилетних возрастных групп от 60 до 94 лет составила 1,0, 1,4, 4,1, 5,7, 13,0, 21,6 и 32,2% соответственно (*). Однако за последнее время сообщается о значительном снижение частоты заболеваемости деменции, что может быть как причиной улучшения качества лечения, так и образования (*), особенно в странах с высоким уровнем дохода (*). Ежегодная смертность от болезни Альцгеймера (основная причина деменции), в зависимости от возраста (45-85+ лет), для США увеличивается с 0,3 до 1131 случая на 100 000 (*).
(2) Да и рак мозга (первичный или вторичный) легче лечить при изоляции мозга от тела. Метод региональной перфузии органов часто используется для лечения рака, например, с применение ультимативных доз вещества без заметных системных побочных эффектов (*, *). В том числе разрабатывается вариант технологии и для головного мозга (*).
(3) Невозможность создания медицинской услуги значительно увеличивающих продолжительность жизни (за видовой предел): а) Прежде всего важно понимать, что не все технологии терапии, которые моно создать, будут созданы. Мы можем вылечить практически любое орфанное моногенное генетическое заболевание, но для большинства из них никогда не будет создано медицинской услуги по их лечению, так как спрос небольшой из-pа редкости болезни и значит коммерчески разработка не обоснована. Да и для ряда генетических заболеваний разработанная терапия снята с производства, так как слишком дорога для потребителя и альтернативные методы ухода и терапии могут уменьшить симптомы заболевания сделав жизнь сносной, но не вылечив болезнь; б) Так же и с терапией старения. Будут симптоматические препараты снимающие проявления старения. относительно дешёвые и пользующиеся огромным спросом. А вот комплексной терапии, действующей на все причин смерти не будет, из-за огромной дороговизны в разработке, еще большей цены проверки и выхода на КИ. И это не смотря на то, что все нужные технологии для этой терапии уже в будут в наличие; в) Благодаря развитию технологий мы создадим разумных существ со значительно большими способностями чем мы сами. Мы результат биологической, слепой эволюции, с большим количеством эволюционного мусора в геноме, который делает нас слабыми. Созданные нами существа не будут иметь данный недостаток, будут продуктом высокотехнологично науки и как результат мы не сможем с ними конкурировать, как неандертальцы с сапиенсам. Другими словами, вся экономическая в том числе медицинская мощь будет развиваться на обслуживание потребностей новых видов, а мы станем неинтересны. Т.е. в начале терапию РПЖ нашего тела мы не успеем разработать, а потом у нас просто не будет нужных мощностей, так как они будут отданы другим видам. К сожалению люди, в том числе трансгуманисты и имморталисты этого не понимают и потому не занимаются проектами ,которые могут действительно создать нужную технологию для радикального продления жизни и сохранения нашего вида, даже в рамках только участка мозга содержащего личность.
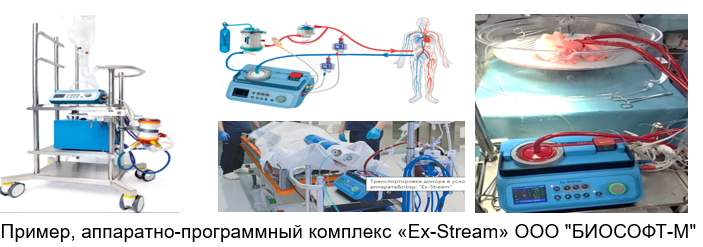
(4) Внедрения перфузионных систем в медицину. Согласно отчёту по глобальному рынку перфузионных услуг ex-vivo, это направление будет значительно расти в период с 2024 по 2030 год. В том числе будет увеличиваться доля машинной перфузии при сохранение органов.
Зачастую, одна и та же перфузионная система может использоваться и для сохранения изолированных органов, и для проведения ЭКМО, и для терапевтической региональной перфузии (in vivo).
Существует 27 стартапов в области систем сохранения органов , включая TransMedics , OrganOx , Paragonix Technologies , Bridge to Life , ADVITOS . Из них 18 стартапов финансируются , 10 из них получили финансирование серии A+. В США больше всего компаний в области систем сохранения органов (14), за ними следуют Швеция и Великобритания, у которых есть (2) компании .
(5) Сделать органы для пересадки бессмертными. Мне тоже приходила в голову идея в начале проверить технологии радикального продления жизни на органах, как лучшей модели с хорошей трансляцией результатов. Ведущий специалист (h-индекс 95, публикации) в области поддержки жизнеспособности органов и создатель первого центра восстановления органов выразился следующим образом: «Мы добиваемся прогресса; теперь мы хотим создать легкое, которое будет служить вечно», — говорит доктор Кешавджи» («UHN marks new era in organ preservation with Ex Vivo Lung Perfusion System») [*].
(6) Аутотрансплантацию органов после восстановления. «Доктор Ашиш Шах, глава отделения кардиохирургии в Университете Вандербильта, где проводится одна из самых оживлённых программ по пересадке сердца в стране, согласился с ним, назвав это «святым Граалем».
«У вас дефектное сердце, — сказал он. — Я вынимаю его. Я помещаю его в свой аппарат. Пока у вас нет сердца, я могу некоторое время поддерживать в вас жизнь с помощью искусственного сердца. Затем я беру ваше сердце и чиню его — клетки, митохондрии, генная терапия, что угодно, — а потом вшиваю его обратно. Ваше собственное сердце. Вот к чему мы стремимся» (The Organ Is Still Working. But It’s Not in a Body Anymore. (2024) Орган все еще работает. Но он больше не в теле [*]. Shah, Ashish H. (резюме, h-индекс 29, публикации).
(7) Метод цифрового двойника. Пока ссылки:
https://pubmed.ncbi.nlm.nih.gov/41295204/, https://pubmed.ncbi.nlm.nih.gov/40996410/, https://pubmed.ncbi.nlm.nih.gov/41044102/, https://pubmed.ncbi.nlm.nih.gov/41047990/, https://pubmed.ncbi.nlm.nih.gov/41072842/, https://pubmed.ncbi.nlm.nih.gov/41075422/, https://pubmed.ncbi.nlm.nih.gov/41166748/, https://pubmed.ncbi.nlm.nih.gov/41192800/, https://pubmed.ncbi.nlm.nih.gov/39920778/
(8) Центры биоинженерной реконструкции органов.
«Целая индустрия развивается вокруг МП органов. Так как невозможно продолжать строить целые операционные для управления одним органом за раз, разрабатываются устройства для автоматизации этих сложных процессов для каждого органа (легкие, печень, почки, сердце), чтобы специалист по перфузии органов мог контролировать и лечить несколько органов одновременно». [*].
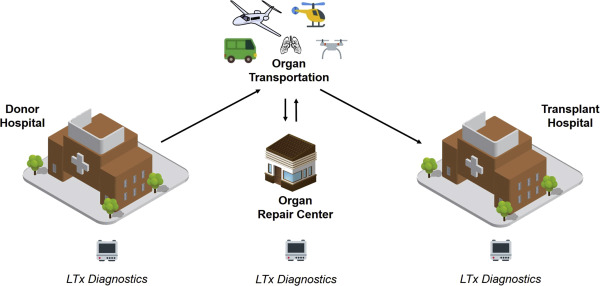
«Представьте себе: внутри больницы Toronto General Hospital находится операционная, которая выглядит так же, как и любая другая, за исключением того, что ни один пациент никогда не будет привезен туда для операции. Пространство заполнено органами — печенью, легкими, сердцем, почками, поджелудочной железой — живущими во множестве странных на вид устройств, которые ремонтируют и регенерируют эти части тела, чтобы их можно было использовать для трансплантации. Хирурги могут войти в комнату, взять орган и выйти так же, как они бы выбрали другие хирургические инструменты или принадлежности. Хотя эта комната пока не существует, в операционной № 11 в Торонтоской больнице общего профиля есть ее уменьшенная версия, где легкие поддерживаются живыми и дышащими и обрабатываются ex vivo – вне тела – перед пересадкой пациенту». [*]
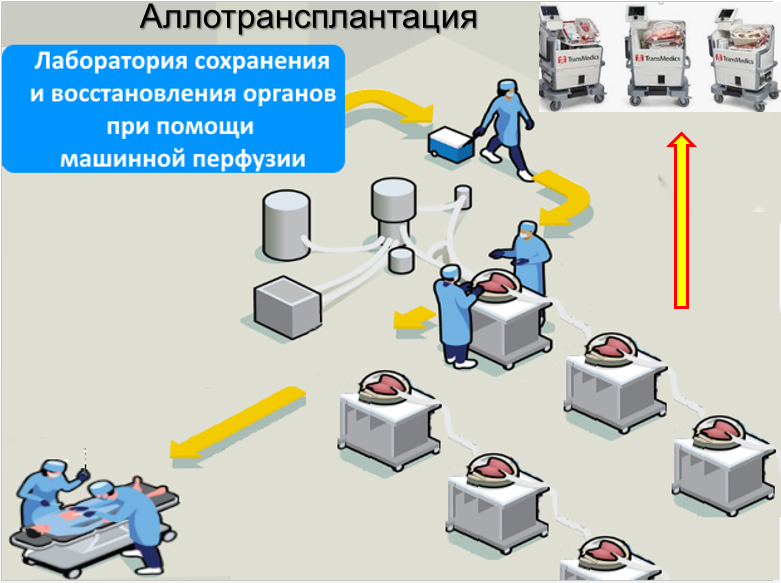
(9) Перфузия изолированной печени (причины выбора на первом этапе). Первый этоп направлен на создание гомеостата, способного поддерживать жизнеспособность органов годами. Выбор печени обусловлен следующими причинами. Это орган который очень сильно востребован в трансплантологии, обладает высокой способностью к регенерации, очень устойчив на перфузионных системах и именно на печени сейчас ставят рекорды по продолжительности перфузии. Именно на базе идеи восстановления печени легче всего создать перфузионную лабораторию ,получит гранты и сделать несколько коммерческих проектов способных профинансировать дальнейшую работу по совершенствованию гомеостатов для перфузии изолированной головы. Кроме того, было показано, что жизнеспособность мозга значительно увеличивается, если в контур перфузионной системы добавить печень [*]. Кроме того, печень (конечно не считая мозга), это практически последний орган для которого ещё не создан искусственный аналог с надлежащей функциональностью.
1_ Длительность перфузии.
Текущий рекорд составляет 17 дней для печени. Для остальных органов в таблице. Более подробная таблица.
| Organ | Days | Date |
| Liver | 17 | 2024 |
| Lungs | 3 | 2024 |
| Heart | 1 | 2022 |
| Kidneys | 4-8 | 2024 |
| Pancreas | ||
| Intestines | 2 | 1971 |
| Limbs | 1 | 2024 |
| Brain | 6 h | 2024 |
| Uterus |
«NMP позволил значительно продлить время консервации для всех типов органов: 24 часа в почках ( 113 _1), 1 неделю в печени ( 114 _1), 3 дня в легких ( 115 _1), 24 часа в сердце ( 116 _1)»
2_ Преимущества машинной перфузии по сравнению с холодовым сохранением
«Крупнейшее РКИ по NMP продемонстрировало 50%-ное снижение показателей отбраковки и 50%-ный более низкий уровень травматизма трансплантата по сравнению с CSP (
24 )».
«Машинная перфузия (МП) печени может уменьшить ишемически-реперфузионное повреждение (ИРИ) и улучшить результаты трансплантации печени (ТП), особенно при использовании трансплантатов от доноров с расширенными критериями (ДКР) [ 1 ]. Преимущества МП были продемонстрированы в нескольких ретроспективных исследованиях [ 2 , 3 , 4 , 5 ] и рандомизированных клинических исследованиях [ 6 , 7 , 8 , 9 , 10 , 11 ]. Многие исследования в настоящее время продолжаются и, вероятно, подтвердят МП как стандарт лечения при ТП, особенно при процедурах РДРВ [ 12 ].»
2_ Недавнее рандомизированное контролируемое исследование показало более высокую выживаемость пациентов через 6 месяцев и 1 год с сердцами DCD, сохраненными EVHP, чем с сердцами, сохраненными SCS [ 77 ].
3. Восстановление органов и ремплантация пока пациенты на сохранение
«Постоянное совершенствование протоколов EVMP, особенно увеличение продолжительности хранения, проложило путь к его более широкому применению, в частности, для восстановления и модификации больных органов, а также для лечения опухолей и инфекций и регенеративных подходов. Более того, внедрение EVMP для доклинических исследований in vivo, улучшающих моделирование заболеваний, вызывает значительный интерес, обеспечивая при этом идеальный интерфейс для биоинженерии и генетических манипуляций. Эти подходы могут применяться не только при аллогенной и ксеногенной трансплантации, но и при аутологичной трансплантации, когда пациенты могут находиться на временной органной поддержке, в то время как больные органы лечатся ex vivo с последующей реимплантацией вылеченного органа. … Представляет трансляционный интерес то, что значительные усилия также прилагаются для изучения инновационных подходов к аутологичным условиям, когда больной орган будет лечиться ex vivo , в то время как пациенту будет предоставлена временная поддержка органа с последующей реплантацией вылеченного органа. Тем временем пациенту проводится временная поддержка органов, такая как гемодиализ для почек или система рециркуляции молекулярного адсорбента для компенсации печени и экстракорпоральная мембранная оксигенация для механической поддержки сердца и легких ( таблица 1 ). В частности, эта процедура предотвращает осложнения, возникающие из-за непропорционального размера органов и вредных побочных эффектов иммуносупрессии, связанных с алло- и ксеногенной трансплантацией, при этом ее своевременность ограничивается только временем сохранения ex vivo . » (***)
«Технология машинной перфузии снижает ишемически-реперфузионное повреждение и позволяет оценить жизнеспособность этих органов, ограничивая процент их выбраковки и улучшая краткосрочные и долгосрочные результаты после трансплантации. Более того, поддерживая метаболическую активность трансплантата, метод нормотермической консервации гарантирует уникальную платформу для проведения регенеративной терапии ex vivo.» (***)
«Недавнее клиническое использование перфузионного устройства ex vivo при трансплантации сердца открывает уникальную возможность лечения сердечных аллотрансплантатов с помощью терапевтических вмешательств для улучшения функции и предотвращения вредных реакций реципиента. …. Эффективная доставка к сердцу терапевтических вмешательств, таких как генная, клеточная или иммунотерапия, является существенным препятствием для клинического применения 4 , 5 . Технология, представленная перфузионными устройствами ex vivo, позволяет непрерывно перфузировать трансплантаты, поддерживая их в нерабочем, но метаболически активном состоянии 6 – 9 . Это дает уникальную возможность лечить все сердце с помощью передовых методов лечения, сводя к минимуму потенциальные побочные эффекты системной доставки 10 – 13 . Еще одним преимуществом использования перфузионных устройств ex vivo для терапевтической доставки является то, что они позволяют вводить лекарства в коронарное кровообращение в течение длительных периодов времени, что невозможно при использовании традиционных методов холодного статического хранения. Это позволяет обеспечить более глобальную доставку терапевтических средств к трансплантату 14 . » (***)
4. Источник органов
«При использовании печени, которую нельзя было использовать в нашем центре для трансплантации, сохранение ex situ достигалось на срок более 7 дней и максимум до 13 дней. » (***)
_18_ Демография доноров. Все донорские печени в Новом Южном Уэльсе, давшие согласие на исследование и отказавшиеся от клинической трансплантации в период с февраля по декабрь 2021 года, рассматривались для включения. Одна печень была уменьшена из-за известной портальной гипертензии в анамнезе, а вторая — из-за цирроза печени. Для разработки протокола перфузировали три целые печени без разделения. Используя наш протокол, 10 донорских человеческих печени были разделены, в результате чего были получены 10 LLSG и 10 ERG, которые были перфузированы на отдельных перфузионных машинах. Что касается разделенной печени, то четыре из десяти печени были получены по пути донорства после смерти мозга (DBD), а шесть были получены по пути донорства после определения смерти по кровообращению (DCD). Причины отказа от донорской печени суммированы в Таблице 1 . Некоторые из этих печени могли быть «пересажены» в других центрах, но протокол нашего исследования не повлиял на решение об их использовании. Причинами отказа от использования печени DBD для трансплантации были: стеатоз, серьезные нарушения функциональных тестов печени, известный билиарный сепсис и плохая промывка печени. Печень DCD не использовалась клинически из-за возраста, превышающего критерии приемлемости DCD в нашем центре (>50 лет) в 3/6, а остальные из-за длительного времени до прекращения кровообращения (>30 мин), морбидного ожирения и острота трансплантационной деятельности. Среднее время холодовой ишемии (CIT, определяемое как время от холодной перфузии до реперфузии с использованием аппарата ex situ) составляло 295 минут (интерквартильный диапазон [IQR] 273–430 минут) (дополнительная таблица 1 ). Для печени с DCD среднее время до смерти (отмена кардиореспираторной поддержки до прекращения кровообращения) составляло 20 минут (IQR 19–29 минут) (дополнительная таблица 1 ).
Легкие от 18 доноров-людей, считавшихся непригодными для трансплантации, подверглись EVLP с перфузатом, содержащим высокодозированные эмпирические антимикробные агенты широкого спектра действия. https://pubmed.ncbi.nlm.nih.gov/24631044/
Здесь мы показываем, что человеческие почки, отбракованные для трансплантации, могут сохраняться в метаболически активном состоянии до 4 дней при перфузии бесклеточным перфузатом, дополненным …. » https://pubmed.ncbi.nlm.nih.gov/38740760/
_10_ .Многие исследовательские группы в значительной степени полагаются на выброшенные человеческие органы для исследований перфузии ex situ , и на протяжении многих лет они были ценным ресурсом для исследований трансплантации. Однако часто невозможно предсказать, станут ли эти органы доступными и когда они появятся; кроме того, вариации в отношении сопутствующих заболеваний и состояний или продолжительности холодовой ишемии довольно значительны, что усиливает уже имеющуюся общую гетерогенность. По этим и другим причинам выброшенные человеческие органы стали непрактичным, менее ценным с научной точки зрения и зачастую ненадежным источником органов. …
5_ Доклиника на человеческой модели. + преимущество перед другими моделями
отя разработано много моделей нормотермической перфузии для органов животных, заметные отличия между видами значительно усложняю интерпретацию результатов полученных на этих моделях. Однако в данном случае, есть возможность работать с органами человека, как умерших пациентов, так и органами, не принятыми к трансплантации или полученными после замены на аллотрансплантат у реципиентов.
Обзор_1: «Доклинические исследования на людях. Возможность сохранения твердых органов в перфузируемой физиологической среде открывает новую область для доклинических исследований, подобных in vivo , с потенциалом ускорения клинического перехода к новым терапевтическим подходам. Таким образом, был разработан большой выбор животных моделей ЭВМП почек, печени и органов грудной клетки, что одновременно облегчает исследование терапевтических схем для различных моделей заболеваний. Однако многочисленные различия, например, между моделями перфузии на грызунах и людях, ограничивают трансляционную значимость этих исследований из-за более низкого перфузионного потока EVMP в моделях на крысах ( 204_1 ) и гиперчувствительности к перфузионным растворам на основе декстрана, чего не происходит у людей ( 205). _1). Более того, широкий спектр заболеваний, в частности, различные модели злокачественных опухолей на животных, все еще не могут быть переносимы из-за сильной гетерогенности туморогенеза ( 206_1 ). Напротив, использование органов умерших пациентов дает возможность протестировать новые фармакотерапевтические методы лечения на соответствующих моделях заболеваний человека и позволяет более точно прогнозировать эффективность терапии по сравнению с моделями на животных. Широкий спектр противовоспалительных агентов (например, кортикостероиды, простагландины, н-ацетилцистеин) дал многообещающие результаты как на моделях грызунов, так и на крупных животных, однако без трансляционной значимости, поскольку клинические испытания не смогли добиться значительной пользы для пациентов ( 209 _1). Напротив, в недавнем исследовании EVMP применяли на донорских легких человека, которые были неприемлемы для трансплантации, чтобы успешно создать модель повреждения легких, вызванного эндотоксемией, путем инстилляции липополисахарида (ЛПС) в легочную артерию ( 210 _1). Этот подход, точно отражающий клинические условия, привел к сильному цитокиновому ответу, а также к снижению содержания кислорода в легочных венах в течение пяти часов, как это наблюдается при ОРДС. Подтверждение концепции ранних фармакологических исследований с использованием EVMP, оценка новой небольшой молекулы BC1215, которая подавляет передачу сигналов NF-κB, в модели ОРДС привела к снижению индукции IL-1, IL-6 и IL-10, измеренного с помощью ELISA. БАЛФ. Кроме того, секвенирование РНК показало, что введение BC1215 после воздействия LPS значительно притупляет транскрипционный ответ NF-κB и сохраняет венозное парциальное давление кислорода ( 210 _1). Помимо оценки эффективности фармакотерапии, EVMP может также поддержать клинические исследования фазы 1 и 2, позволяющие определить органоспецифичные побочные эффекты, которые имеют решающее значение для клинического перехода. Например, обычно используемые модели на животных для проверки гепатотоксичности новых лекарств демонстрируют значительные различия с человеческими условиями из-за различий в метаболизме лекарств и в основном однородных экологических и генетических условий у инбредных линий животных. Напротив, модель EVMP, исследующая влияние повреждения печени, вызванного ацетаминофеном, использовала ткань печени человека из частичных резекций печени для имитации клинических условий. Примечательно, что система EVMP позволяла ежечасно отбирать пробы перфузата и оценивать в реальном времени клинические параметры, показывающие нарушение функции печени во время отравления APAP с более низким потреблением глюкозы и скоростью производства лактата при сохраненной способности синтеза гепатоцитов ( 211 _1). Следует отметить, что оценка функции печени по клиренсу индоцианина зеленого выявила стабильную гепатоцеллюлярную функцию в течение всего периода перфузии, что указывает на клинически значимую ситуацию ( 211 _1). Наконец, использование моделей EVMP для инициирования клинических испытаний может снизить этическое бремя тестирования новых фармакологических препаратов, тем самым ускоряя переход многообещающих кандидатов в клиники ( рис. 1H ).»
_13_ Современные 2D-культуры in vitro и модели на животных представляют собой серьезные ограничения в воспроизведении физиопатологии человека с поразительными расхождениями в оценке эффективности лекарств и побочных эффектов по сравнению с исследованиями на людях.
_19_»По мере того, как мы продвигаемся дальше в эпоху персонализированной медицины, проблема разработки клинически прогностических модельных систем для оценки технологий переноса генов и редактирования генов представляет собой серьезное препятствие. Идеальная модельная система должна не только точно имитировать физиологические состояния человека и сложную организацию тканей, но и надежно предсказывать клинические результаты. В мире генной терапии, направленной на печень, 2D и 3D модели in vitro, включая органоиды, полученные из индуцированных плюрипотентных стволовых клеток (iPSC), мышиные модели, включая модели ксенотрансплантатов, и приматов, не являющихся человеком, традиционно использовались для разработки и проверки новых передовых терапевтических средств. . Однако, учитывая тот факт, что печень является сложным органом, состоящим из нескольких типов клеток, которые вносят вклад в уникальную структурную и функциональную организацию, сложность человеческой печени оказалось трудно переосмыслить. В ответ на этот вопрос, особенно в отношении терапии на основе аденоассоциированных вирусных (AAV) векторов, нацеленной на печень, мы представляем разработку доклинической модели, основанной на целых эксплантатах печени человека, хранящихся в нормотермической (36 °C) перфузии ex situ. система. Эта модель обеспечивает платформу, которая позволила нам впервые, насколько нам известно, оценить функциональность существующих и дополнительных рекомбинантных аденоассоциированных вирусных (rAAV) векторов непосредственно в печени человека…. Модель, включающая человеческий орган, снабжаемый человеческой кровью и поддерживающий температуру тела, предлагает поразительно точное приближение к физиологическим условиям человека. Можно утверждать, что существует несколько альтернатив, которые приближают нас к человеческой среде, если не считать реальных клинических испытаний. Это означает исключительный потенциал этой модели в ускорении прогресса в области генной терапии, опосредованной печенью – как вирусной, так и потенциально невирусной – путем проведения исследований, которые точно имитируют клинические сценарии, в которых в конечном итоге будет применена генная терапия. Учитывая сложность и потенциальные этические вопросы, связанные с этой моделью, необходимо подчеркнуть, что основной целью донорской печени является трансплантация, целью которой является предоставление прямой помощи по спасению жизни нуждающимся реципиентам. ….
Наконец, модель эксплантата печени человека ex situ открывает захватывающие возможности для разработки различных векторов AAV с помощью подходов направленной эволюции. Его уникальная особенность сохранения нативной структуры печени и внеклеточного матрикса человека делает его идеальной платформой для совершенствования стратегий, таких как детаргетинг HSPG, описанный ранее в гуманизированной модели FRG 19 .
В целом, мы считаем, что эксплантат печени человека является одной из наиболее биологически и клинически прогнозируемых доклинических моделей, доступных сегодня, поскольку он предоставляет ценную возможность для развития и оценки вектора в контексте всего органа с неповрежденной архитектурой и зонированием органа. наличие человеческой крови.».
Пример источника печение человека для исследований
10_ С распространением новых подходов и технологий в области перфузии и регенерации органов необходимы доклинические исследования для разработки, оценки и внедрения в клиническую практику, поскольку они предлагают хорошо контролируемые условия, которые позволяют исследовать основные молекулярные механизмы ( 1 )…. Модели на свиньях оказались очень успешными и полезными в доклинических исследованиях в области трансляционной трансплантации, особенно при разработке перфузионных технологий. Свиньи имеют анатомию брюшной полости, висцеральных и сосудистых органов, аналогичную человеческой, с органами аналогичного размера и, следовательно, представляют собой превосходную модель крупных животных при трансплантации ( 2 ). Кроме того, геномное сходство с человеком, особенно в отношении иммунной системы и экспрессии белков, связанных с воспалением, также увеличивает ценность этой конкретной модели ( 3 ). …
Учитывая явные преимущества модели со свиньями, резко возросло развитие многих видовоспецифичных лабораторных ресурсов со специфическими антителами, анализами и наборами, которые облегчили углубленный молекулярный анализ и позволили изучить множество новых направлений исследования. расследование.
Несмотря на научные преимущества моделей на крупных животных, остаются серьезные этические проблемы, а приемлемость экспериментов на животных остается весьма спорной и, следовательно, жестко регулируется. Чтобы соответствовать строгим этическим стандартам, многие исследовательские группы сталкиваются с непомерно высокими затратами, связанными с животноводством и крупными экспериментами на животных ( 4 ). Несмотря на захватывающую и быстро развивающуюся область, прекрасную доклиническую модель и крупные технические достижения, направленные на решение важной клинической проблемы, возможности исследований ограничиваются этическими и экономическими барьерами.
Мы предполагаем, что разработка надежного и эффективного процесса закупки органов свиней на бойне станет работоспособным решением для многих исследовательских групп. Использование ресурсов бойни не только выгодно с этической точки зрения, но и соответствует принципу «замены» в рамках 3R (сокращение, замена и усовершенствование), которые образуют этическую основу для научных исследований на животных ( 5 ). Он также предоставляет органы, полученные от модели животного, что очень похоже на клинический сценарий донорства после сердечно-сосудистой смерти (DCD), что является основным направлением внимания при расширении пула доноров в исследованиях трансплантации. … Хотя органы свиней со скотобойни использовались в многочисленных экспериментах по перфузии ex vivo ( 6-8 ) , стандартизированная методология извлечения нескольких органов еще не описана. Здесь мы сообщаем о процедуре закупки нескольких органов, которая использует стандартизированный подход и обеспечивает жизнеспособные органы, которые представляют собой модель DCD и могут быть использованы при разработке перфузии органов ex vivo …. Наша группа провела 81 закупку среди нескольких органов, используя описанную методологию для получения успешных, воспроизводимых и эффективных результатов закупок, обобщенных вТаблица 1. По нашему опыту, время от обескровливания до начала холодной перфузии или времени теплой ишемии (WIT) обычно занимает от 12 до 20 минут, но должно быть завершено менее чем за 30 минут, чтобы быть приемлемым для экспериментальной нормотермической перфузии. Однако, как показала ранее опубликованная работа, WIT менее 60 минут имеет высокие показатели выживаемости (в модели трансплантации) при лечении нормотермической машинной перфузией (NMP) ( 10-12 ) .
_22_ Возможность перевода продлевающих жизнь фармакологических методов лечения между разными видами
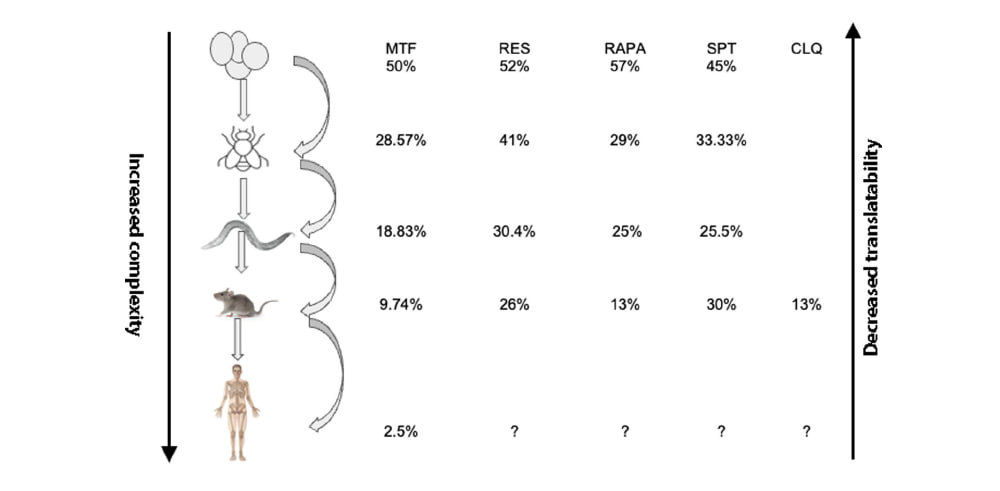
_»
На первый взгляд артерии крысы ex vivo ведут себя аналогично артериям человека. Исследования показали, что ткани крыс вызывают те же изменения сократимости, что и люди, в отношении обычных вазоконстрикторов и вазодилататоров и даже в отношении многих других, менее часто используемых препаратов, таких как каннабидиол (КБД),6 мевалонат7 и FK506.8.
Когда Барановска-Кучко и др. изучив реакцию артерий крысы и человека на КБД, они обнаружили, однако, что за наблюдаемыми реакциями релаксации стоят разные фармакологические механизмы.2 У людей реакция была эндотелиально-зависимой и опосредована рецепторами KCa и IP, EP4 и TRPV1.2 Но у крыс расслабление было независимым от эндотелия и опосредовано рецептором CB1, что позволяет предположить разный механизм действия между крысами и людьми.2 https://www.reprocell.com/blog/biopta/rat-aorta
_13_ Сегодня исследования лекарств основаны на использовании традиционных 2D-культур клеток in vitro и экспериментах на животных, которые не позволяют должным образом предсказать клиническую эффективность, токсичность и побочные эффекты терапии у людей , поскольку они неадекватны для воспроизведения физиологии человека
Органы на чипах
(позитивный результат не означает быстрое введение в клиническую практику, в отличие от результатов на целых органах. Восстановленные органы востребованы в трансплантологии)
_13_ Технологии «Органы на чипах» (ООС) это миниатюрная микрофизиологическая система для биомедицинских исследований призванная обеспечить ресурсоэффективный ответ на главные вопросы биомедицинского поиска : 1) лучшее понимание механизмов заболеваний и связанных с ними патологических процессов; 2) разработка эффективных терапевтических стратегий лечения заболеваний с ограниченными побочными эффектами и влиянием на условия жизни.
Рис. 3

Рис. 3 . Преимущества одной и нескольких ООС-платформ по сравнению с другими методологиями.
«Современные методологии разработки лекарств имеют серьезные ограничения в способности надлежащим образом учитывать сложную физиопатологию тканей человека in vivo. Как традиционная 2D-культура, так и (дорогостоящие) модели животных не обеспечивают точных прогнозов относительно клинических результатов у людей с поразительными расхождениями в эффективности и побочных эффектах по сравнению с испытаниями на людях (Дхиман и др., 2019; Рен и др., 2020 г.; Нам и др., 2015 ). Это приводит к высоким затратам и низкому уровню успеха при внедрении в клинику, что является причиной снижения числа одобренных препаратов, увеличения продолжительности процесса разработки препаратов и более высокого риска отзыва препарата с рынка перед лицом огромных инвестиций (Радхакришнан и др., 2020 г.).» https://www.sciencedirect.com/science/article/pii/S0956566323002130?via%3Dihub
подборка по теме https://nestarenie.ru/part_7.html
6. Универсальность системы
Зачастую, одна и та же перфузионная система может использоваться и для сохранения изолированных органов, и для проведения ЭКМО, и для терапевтической региональной перфузии (in vivo).
PBS® (Medtronic), изначально разработанный для сердечно-легочного шунтирования или экстракорпоральной мембранной оксигенации, также использовался для клинической печеночной HMP (4°C–6°C). Он обеспечивает пульсирующий поток при использовании раствора Vasosol Organ Perfusion. Клинические исследования PBS продемонстрировали снижение продукции провоспалительных цитокинов ( 26 ).
Устройство Lung Assist™ … . Дополнительный интерес представляет то, что оно позволяет проводить изолированную перфузию in и ex vivo как в гипотермических, так и в нормотермических условиях (12°C–37°C). Аппарат ИВЛ не входит в комплект устройства, однако любой уже существующий аппарат ИВЛ совместим для использования

7. Историческая справка
Позже я заполню этот раздел. Сама история создания таких систем в России (см. Гомеостат) и в мире в целом (Алексис Каррель, Чарльз Линдберг) очень интересна. Но многие технические решения устарели и оценить их потенциал на фоне современных технологий, которые созданы за последние 5 лет достаточно сложно.
+
/Белзер и др. (2 ) разработали гипотермический пульсирующий перфузионный аппарат для сохранения почек собак в течение 72 часов. Также Бреттшнайдеру и Старцлю (
3 ) удалось успешно перфузировать печень собак в течение 8–24 часов перед трансплантацией./
8. Комплекс органов
_ The novel in vitro reanimation of isolated human and large mammalian heart-lung blocs
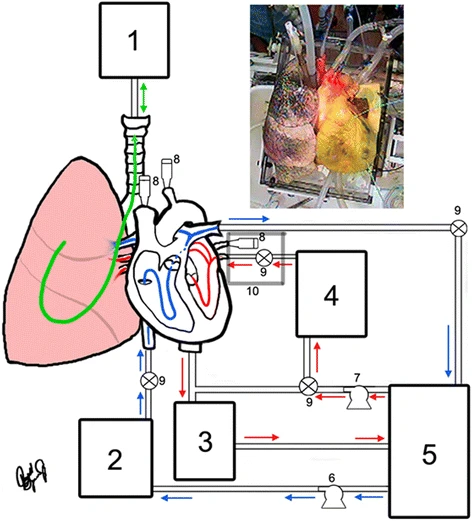
9. Выживаемость аллотрансплантатов.
«Однако продолжительность жизни аллотрансплантатов не соответствует ожидаемой продолжительности жизни пациентов. Двадцать процентов реципиентов потеряют свой трансплантат в течение 5 лет, а 50% — в течение 10–12 лет. Многие другие органы переживают худшие времена; например, выживаемость аллотрансплантата легких в течение 5 лет составляет всего 50% ( http://optn.transplant.hrsa.gov ). «https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5490786/
_12 Попытки улучшить сохранность конечностей для трансплантации с помощью перфузии ex vivo дали многообещающие результаты. Однако повсеместно отмечаются метаболический ацидоз, аберрантная биохимия перфузата и значительный отек, вызванный перфузией. Поэтому оптимизация протоколов перфузии необходима для поддержания здоровья тканей. ….
Васкуляризованная композитная аллотрансплантация (VCA) значительно улучшает качество жизни пациентов с потерей конечностей 1 . Однако серьезные нежелательные явления встречаются часто, в первую очередь из-за профилактической иммуносупрессии, необходимой для контроля острого отторжения. Несмотря на это, частота острого отторжения после VCA выше, чем при любой другой процедуре трансплантации: 85 процентов трансплантатов отторгаются в течение первых 12 месяцев 2 . Повторное отторжение приводит к значительному фиброзу мягких тканей, что делает конечность нефункциональной. Отторжение VCA представляет собой сложный, многогранный процесс, включающий иммунные компартменты резидентного донора, клеточное повреждение внутри трансплантата, аллорераспознавание и клональную экспансию аллореактивных Т-клеток реципиента 3 . Вполне вероятно, что повреждение трансплантата в результате донорской операции, гипотермии, ишемии и реперфузии способствует посттрансплантационному воспалению и иммунореактивности. Таким образом, улучшение этапов сохранения VCA с целью уменьшения повреждения трансплантата имеет важное значение.
2_ После трансплантации сердца у 10–20% донорских трансплантатов развивается первичная дисфункция трансплантата (ПГД), что приводит к 39% смертности через 1 месяц после трансплантации [ 53 , 54 ].
ПЕЧЕНЬ
_20_ Несмотря на широкий успех трансплантации печени и улучшение иммуносупрессии, острое отторжение печени наблюдается у 25% пациентов на ранних этапах после трансплантации, что способствует значительной заболеваемости [ 52 ].
Лёгкие
Острое отторжение после трансплантации легких, 2024, https://pubmed.ncbi.nlm.nih.gov/38656281
10. На сохранение без органа
Его больные легкие были полностью удалены из его тела, «искусственное легкое» выполнило свою работу, а два грудных имплантата размером DD служили заполнителями в его грудной полости, поддерживая его сердце. Днем позже во время второй операции ему в грудь трансплантировали донорские легкие. https://www.npr.org/sections/health-shots/2023/11/12/1212306197/double-lung-transplant-flu-vaping-dd-breast-implants
https://edition.cnn.com/2016/06/10/health/artificial-heart-555-days-transplant/index.html Ожидая пересадки человеческого сердца, Стэн Ларкин прожил 555 дней вообще без органа.
11. Нехватка органов и расширение списка допустимых к трансплантации органов
_4_ Однако существует огромное несоответствие между доступными донорскими органами и пациентами, имеющими спрос, что приводит к высокой смертности в листах ожидания ( 1 ). Чтобы преодолеть это неравенство, центры трансплантации расширили свои критерии отбора ( 2–4 ), и лишь немногие страны легализовали донорство после сердечно-сосудистой смерти (DCD), за исключением донорства после смерти мозга (DBD) .
_5 Тем не менее, доступные донорские трансплантаты ограничены, и пациенты остаются в списке в течение многих лет с повышенным риском смерти до трансплантации. 5
_6 Двадцать процентов реципиентов потеряют взятку в течение пяти лет, а 50% — в течение 10–12 лет ( 220 ).
_6 В 2020 году Сеть по закупкам и трансплантации органов сообщила, что в листах ожидания на трансплантацию органов в США стояли 116 577 пациентов ( 227 ). В среднем 20 пациентов в списке ожидания умирают каждый день из-за нехватки донорских органов ( 228 ).
_10_ На сегодняшний день проблема увеличения пула доноров в основном решается за счет использования органов доноров с расширенными критериями (ECD) более старых и повышенного риска, но они часто дают худшие результаты по сравнению с органами, полученными от доноров со стандартными критериями (SCD).
_20_ Во всем мире также наблюдается нехватка доноров органов: 15% пациентов умирают, находясь в списке ожидания трансплантации печени [ 65 ]. Доступные донорские трансплантаты стали основным ограничивающим фактором, поскольку спрос превышает предложение. …
В целях увеличения пула доноров и удовлетворения растущего спроса за последние 20 лет использовались доноры с расширенными критериями, извлекающие и имплантирующие трансплантаты от доноров с маргинальным/высоким риском, таких как пожилые доноры с сопутствующими заболеваниями и доноры после сердечно-сосудистой смерти ( ДКД). Доноры из группы высокого риска увеличивают доступность донорских органов, но имеют большую восприимчивость к ишемическим реперфузионным повреждениям, что приводит к увеличению заболеваемости и смертности [ 16 ].
Это потребовало принятия инновационных технологий и стратегий для защиты этих трансплантатов повышенного риска от вредного воздействия традиционных методов консервации и ишемически-реперфузионного повреждения (ИРИ) [ 66 ].
12. старение и трансплантация
Я заявляю. молодой орган будет оказывать благотворное влияние на старый организм.
Критики. под действие старого организма молодой орган скоро «постареет».
Ответ
Конечно старый организм негативно влияет на органы, в том числе после их омоложения /восстановления. Только технологии не стоят на месте и можно модифицировать орган, чтоб он стал устойчив к пагубному воздействию разрушающего сигналинга от старого организма и оказывал более выраженное омолаживающее действие.
Кроме того, исследования показывают:
«
сбор материала.
Статьи.
Влияние возраста донора на трансплантацию органов: обзор и выводы для исследований старения.
Трансплантация старых органов способствует старению у молодых реципиентов.
Несоответствие возраста донора и реципиента: потенциал переноса старения.
Влияет ли возраст донора на биомаркеры старения у пациентов, перенесших трансплантацию почки?
Репликативное старение и артериосклероз после трансплантации почки.
Клеточное старение и хрупкость при трансплантации.
О старых органах пересаженных молодым.
Почему нет до сих пор длительной / неограниченной по времени перфузии?
_1_ NMP has enabled a significant prolongation of preservation times throughout all organ types with 24 h in kidney (113), 1 week in liver (114), 3 days in lung (115), 24 h in heart (116) EVMP.
- Инфекции
_9_ Возможность продления NMP на несколько дней, впервые предложенная группой из Цюриха [ 100 , 101 , 102 ], может стать ключом к расширению терапевтического окна для достижения эффективности терапии регенерации органов [ 103 , 104 , 105 ].
_12 Попытки улучшить сохранность конечностей для трансплантации с помощью перфузии ex vivo дали многообещающие результаты. Однако повсеместно отмечаются метаболический ацидоз, аберрантная биохимия перфузата и значительный отек, вызванный перфузией. Поэтому оптимизация протоколов перфузии необходима для поддержания здоровья тканей. ….
Васкуляризованная композитная аллотрансплантация (VCA) значительно улучшает качество жизни пациентов с потерей конечностей 1 . Однако серьезные нежелательные явления встречаются часто, в первую очередь из-за профилактической иммуносупрессии, необходимой для контроля острого отторжения. Несмотря на это, частота острого отторжения после VCA выше, чем при любой другой процедуре трансплантации: 85 процентов трансплантатов отторгаются в течение первых 12 месяцев 2 . Повторное отторжение приводит к значительному фиброзу мягких тканей, что делает конечность нефункциональной. Отторжение VCA представляет собой сложный, многогранный процесс, включающий иммунные компартменты резидентного донора, клеточное повреждение внутри трансплантата, аллорераспознавание и клональную экспансию аллореактивных Т-клеток реципиента 3 . Вполне вероятно, что повреждение трансплантата в результате донорской операции, гипотермии, ишемии и реперфузии способствует посттрансплантационному воспалению и иммунореактивности. Таким образом, улучшение этапов сохранения VCA с целью уменьшения повреждения трансплантата имеет важное значение.
_14_ Продолжительность перфузии. Оптимизация продолжительности перфузии может стать решающим шагом в увеличении преимуществ правильно спроектированных перфузатов. Как было успешно продемонстрировано в клинических исследованиях, короткий период ЭВНП (до 2 часов) приемлем после периода СКС ( 6 , 7 , 11 , 49 ). Однако непрерывная нормотермическая перфузия с момента извлечения может позволить полностью избежать холодового ишемического повреждения. Недавние исследования DCD на свиньях подтвердили осуществимость и безопасность длительного EVNP с почти полным исключением SCS с использованием перфузатов цельной крови в течение 10 часов в печени ( 33 , 50 ) и бесклеточного раствора Стена в течение 12 часов в легких ( 51 ). Первоначальные данные о почках показали, что непрерывная 8-часовая EVNP осуществима и безопасна для трансплантатов почек донора с работающим сердцем хорошего качества ( 52 ), а в последующем исследовании на свиных почках DCD та же группа продемонстрировала, что непрерывная 16-часовая EVNP EVNP с почти полным исключением SCS превосходил кратковременный EVNP после SCS ( 28 ). Кроме того, было показано, что субнормотермическая 24-часовая консервация с использованием бесклеточного раствора Стена поддерживает низкое и стабильное сосудистое сопротивление, обеспечивая при этом адекватную гистологическую консервацию в почках свиней DCD ( 12 ).
_18_ При использовании печени, которую нельзя было использовать в нашем центре для трансплантации, сохранение ex situ достигалось на срок более 7 дней и максимум до 13 дней.
Нехватка органов и расширение списка допустимых к трансплантации органов.
_4_ Однако существует огромное несоответствие между доступными донорскими органами и пациентами, имеющими спрос, что приводит к высокой смертности в листах ожидания ( 1 ). Чтобы преодолеть это неравенство, центры трансплантации расширили свои критерии отбора ( 2–4 ), и лишь немногие страны легализовали донорство после сердечно-сосудистой смерти (DCD), за исключением донорства после смерти мозга (DBD) .
_5 Тем не менее, доступные донорские трансплантаты ограничены, и пациенты остаются в списке в течение многих лет с повышенным риском смерти до трансплантации. 5
_6 Двадцать процентов реципиентов потеряют взятку в течение пяти лет, а 50% — в течение 10–12 лет ( 220 ).
_6 В 2020 году Сеть по закупкам и трансплантации органов сообщила, что в листах ожидания на трансплантацию органов в США стояли 116 577 пациентов ( 227 ). В среднем 20 пациентов в списке ожидания умирают каждый день из-за нехватки донорских органов ( 228 ).
_10_ На сегодняшний день проблема увеличения пула доноров в основном решается за счет использования органов доноров с расширенными критериями (ECD) более старых и повышенного риска, но они часто дают худшие результаты по сравнению с органами, полученными от доноров со стандартными критериями (SCD).
_20_ Во всем мире также наблюдается нехватка доноров органов: 15% пациентов умирают, находясь в списке ожидания трансплантации печени [ 65 ]. Доступные донорские трансплантаты стали основным ограничивающим фактором, поскольку спрос превышает предложение. …
В целях увеличения пула доноров и удовлетворения растущего спроса за последние 20 лет использовались доноры с расширенными критериями, извлекающие и имплантирующие трансплантаты от доноров с маргинальным/высоким риском, таких как пожилые доноры с сопутствующими заболеваниями и доноры после сердечно-сосудистой смерти ( ДКД). Доноры из группы высокого риска увеличивают доступность донорских органов, но имеют большую восприимчивость к ишемическим реперфузионным повреждениям, что приводит к увеличению заболеваемости и смертности [ 16 ].
Это потребовало принятия инновационных технологий и стратегий для защиты этих трансплантатов повышенного риска от вредного воздействия традиционных методов консервации и ишемически-реперфузионного повреждения (ИРИ) [ 66 ]. Чтобы улучшить результаты этих расширенных донорских трансплантатов, много инвестиций и исследований было посвящено таким применениям, как нормотермическая и гипотермическая машинная перфузия. Хотя первоначальные исследования показывают, что эти технологии имеют преимущества, большое влияние оказывают затраты и необходимая техническая поддержка, в то время как доказательства преимуществ, ориентированных на пациента, остаются неясными. Для окончательной оценки этого необходимы дальнейшие испытания. Нормотермическая машинная перфузия еще не продемонстрировала преимущества для пациентов, включая снижение смертности, сокращение пребывания в больнице, продление трансплантата и/или выживаемость пациентов [ 67 ]. Исследование перфузионного использования печени (PLUS) в настоящее время оценивает, улучшает ли нормотермическая машинная перфузия (NMP) использование органов без ущерба для результатов в печени с расширенными критериями. Эта тема обсуждается более подробно в других разделах этого специального выпуска [ 68 ].
СЕРДЦЕ
Смертность после пересадки сердца?
2_ После трансплантации сердца у 10–20% донорских трансплантатов развивается первичная дисфункция трансплантата (ПГД), что приводит к 39% смертности через 1 месяц после трансплантации [ 53 , 54 ].
Преимущества EVHP по сравнение с другими типами сохранения сердец
2_ Недавнее рандомизированное контролируемое исследование показало более высокую выживаемость пациентов через 6 месяцев и 1 год с сердцами DCD, сохраненными EVHP, чем с сердцами, сохраненными SCS [ 77 ].
ПЕЧЕНЬ
_20_ Несмотря на широкий успех трансплантации печени и улучшение иммуносупрессии, острое отторжение печени наблюдается у 25% пациентов на ранних этапах после трансплантации, что способствует значительной заболеваемости [ 52 ].
Лёгкие
Острое отторжение после трансплантации легких, 2024, https://pubmed.ncbi.nlm.nih.gov/38656281
Литература Часто задаваемые вопросы
—————————————
предлагая глубокое понимание заболеваний печени и потенциальных последствий для исследований и терапевтических разработок.
+
Длительная машинная перфузия разделенной человеческой печени: новая модель для регенеративных и трансляционных исследований. https://pubmed.ncbi.nlm.nih.gov/39532864/
+
Новая эксплантированная модель печени человека для оценки печеночной экстракции, желчевыделения и транспортной функции. https://pubmed.ncbi.nlm.nih.gov/37042227/
Наши результаты показали, что NMP из больной эксплантированной печени человека является превосходной моделью для оценки печеночной экстракции, клиренса, желчной экскреции и DDI.
Отбракованные органы и МП
Критическая оценка отбракованной донорской печени в регионе евротрансплантации: потенциальные последствия для машинной перфузии . https://pubmed.ncbi.nlm.nih.gov/36927714/
Наши данные свидетельствуют о том, что многие отклоненные донорские печени имеют потенциал для оценки с помощью машинной перфузии. Всестороннее использование машинной перфузии необходимо и полезно для устранения текущей нехватки органов.
+
Тестирование отбракованной печени методом нормотермической машинной перфузии в исследовании VITTAL: вторичные конечные точки и 5-летние результаты. https://pubmed.ncbi.nlm.nih.gov/38109282/
Нормотермическая машинная перфузия (НМП) позволяет проводить предтрансплантационную оценку печени доноров высокого риска. Испытание VITTAL продемонстрировало, что 71% в настоящее время выбрасываемых органов могут быть трансплантированы со 100% 90-дневной выживаемостью пациентов и трансплантатов.
+
Легкие от 18 доноров-людей, считавшихся непригодными для трансплантации, подверглись EVLP с перфузатом, содержащим высокодозированные эмпирические антимикробные агенты широкого спектра действия. https://pubmed.ncbi.nlm.nih.gov/24631044/
Отработка технологии перфузии (основная статья)
Поиск терапевтических технологий
Восстановление трансплантата во время машинной перфузии: современный обзор стратегий.
https://pubmed.ncbi.nlm.nih.gov/38726753
+
Различные биологические модели
Таким образом, модель крысы может быть использована для прогнозирования пероральной абсорбции лекарств в тонком кишечнике человека, но не для прогнозирования метаболизма лекарств или пероральной биодоступности у человека.
https://pubmed.ncbi.nlm.nih.gov/16841194
Нормотермическая ex vivo печеночная платформа с использованием печени свиней, забитых на бойнях, для моделирования заболеваний. https://pubmed.ncbi.nlm.nih.gov/36135018/ (отработка методов тестирования)
Машинная перфузия печени и модели животных in vivo: систематический обзор ландшафта доклинических исследований. https://pubmed.ncbi.nlm.nih.gov/38329986/ ( изучение методологических и отчетных стандартов с использованием оценки ARRIVE (Исследования на животных: Отчетность об экспериментах in vivo). )
Имеются данные, что менее трети исследований на животных переносится в испытания на людях [ 31 , 32 ].
- 31.Gurusamy KS, Moher D., Loizidou M., Ahmed I., Avey MT, Barron CC и др., Оценка клинической значимости инструмента доклинических исследований животных (RAA): разработка и объяснение. PeerJ, 2021. 9: стр. e10673. doi: 10.7717/peerj.10673 [ DOI ] [ Бесплатная статья PMC ] [ PubMed ] [ Google Scholar ]
- 32.Хакэм, М. Дэниел Г. и Редельмейер М. Дональд А., Перевод исследовательских данных с животных на людей. Американская медицинская ассоциация, 2006. Том 296 (№ 14): стр. 1731–1732. [ DOI ] [ PubMed ] [ Google Scholar ]
Исправление: Нормотермическая машинная перфузия печени свиньи : методологическая основа и потенциальные подводные камни: Исправление. https://pubmed.ncbi.nlm.nih.gov/35506016/
Нормотермическая машинная перфузия печени свиньи : методологическая основа и потенциальные подводные камни. https://pubmed.ncbi.nlm.nih.gov/34912950/
Забор органов из брюшной полости у свиней, забитых на бойнях: индивидуальная модель донорства органов после остановки кровообращения для перфузии органов ex vivo, соответствующая принципам «трех R» (сокращение, замена и уточнение). https://pubmed.ncbi.nlm.nih.gov/35242846/
Терминальная заготовка крови у свиней с помощью острой нормоволемической гемодилюции для перфузии органов ex vivo . https://pubmed.ncbi.nlm.nih.gov/34879898/
Ex vivo функциональный целый орган в биомедицинских исследованиях: обзор https://pubmed.ncbi.nlm.nih.gov/39592544/
Органоиды / «орган-на-чипе»
Новые, инновационные модели для изучения окислительно-восстановительных повреждений, связанных с ишемией/реперфузией при трансплантации органов. https://pubmed.ncbi.nlm.nih.gov/36670893/
Центр восстановления органов и реимплантация
Реимплантация
Эти подходы могут применяться не только в условиях аллогенной и ксеногенной трансплантации, но и в условиях аутологичной трансплантации, когда пациенты могут находиться на временной поддержке органов, пока больные органы лечатся ex vivo , а затем следует реимплантация вылеченного органа.
Трансляционный интерес представляют также значительные усилия по исследованию инновационных подходов для аутологичных условий, где больной орган будет лечиться
ex vivo , в то время как пациент подвергается временной поддержке органа с последующей реплантацией вылеченного органа. В то же время пациент подвергается временной поддержке органа, такой как гемодиализ для почки или система рециркуляции молекулярного адсорбента для компенсации печени и экстракорпоральная мембранная оксигенация для механической поддержки сердца и легких (
таблица 1 ). В частности, эта процедура исключает осложнения, возникающие из-за непропорционального размера органа и пагубных побочных эффектов иммуносупрессии, связанных с алло- и ксеногенной трансплантацией, при этом ее временные ограничения ограничиваются только временем сохранения
ex vivo .
«Центры восстановления человеческих органов: факт или вымысел?«
Уитсон, Комментарий: Центры ARC органов: Центры оценки и восстановления при трансплантации как шлюзы к значимым терапевтическим вмешательствам., JTCVS Open, № 3, с. 173
https://doi.org/10.1016/j.xjon.2020.08.004
_20_ Развитие трансплантологии было сосредоточено на сохранении донорских органов в том состоянии, в котором они были эксплантированы, и смягчении процесса их деградации. Современные стратегии наряду с биоинженерными подходами нацелены на терапию донорских органов ex vivo, чтобы попытаться создать трансплантаты, превосходящие то состояние, в котором они были первоначально обнаружены. Lung Bioengineering 1 (LB1) — одна из таких новаторских коммерческих компаний, занимающихся восстановлением легких для клинической трансплантации. Только LB1 и его партнер LB2 способны потенциально покрыть потребности в перфузии легких на всех континентах [ 77 ]. Идея создания этих центров восстановления органов заключалась бы в том, чтобы использовать возможность применения диагностики и терапии к маргинальным трансплантатам во время перфузии органов ex vivo, включая печень, модифицированную терапией стволовыми клетками, модификацией генов, манипулированием иммунными реакциями, а также использовать точные фармакологические и биологические методы лечения. [ 78 ]. В Великобритании исследования и инвестиции в ARC являются важным событием и описываются как стремление национальной стратегии трансплантации (NHSBT), в которой донорская печень является ключевой целью [ 79 ].
Вопросы физиологии (основная статья)
сравнительная анатомия — https://www.frontiersin.org/journals/physiology/articles/10.3389/fphys.2021.693735/full
https://www.niehs.nih.gov/research/resources/visual-guides/guides/heart-sternum-diaphragm
https://www.elsevier.com/resources/anatomy
https://www.sciencedirect.com/science/article/pii/S0925443918301893?via%3Dihub
langendrf +viideo
https://app.jove.com/ru/v/202130/cardiac-graft-procurement-for-langendorff-perfusion
https://www.hope-liver.com/concept (печень)
Воздействия на орган
1_ Разные температуры. Гипотермический, нормотермический, гипертермический.
2_ Разная скорость потока перфузата через сердце.
3_ Разное подаваемое давление перфузата либо регуляция давления самим сердцем.
4_ Электростимуляция, регуляция частоты сокращений. (статья)
5_ Магнитное поле.
6_Дозаторы под вещества, в том числе смеси с клетками, вирусными векторами и т.п. Крепить через краник. см. Пример _1, видео введения препарата. , «после локализации внутривенно введенных магнитных микрочастиц в полости правого желудочка с помощью внешнего электромагнита«
7_ Хим анализ
8_ вращение сердца (сейчас популярная тема) О влияние вращения — https://t.me/myoxys/348
9_ Облучение. Совместимая с томографической микроскопией система Лангендорфа для динамической структурной характеристики сердечного цикла- https://www.frontiersin.org/journals/cardiovascular-medicine/articles/10.3389/fcvm.2022.1023483/full
10_ микроэлектродной матрицы (MEA) — https://www.youtube.com/watch?v=wNzt6kluQ5I
Примеры лабораторий
Пример лаборатории — https://bmiorganbank.com/perfusion-research-expert-services/
Еще пример лаба для тестирования лекарственных веществ на перф органах — https://www.tno.nl/en/newsroom/insights/2023/03/ex-vivo-organ-perfusion-data/
Еще пример? https://utswmed.org/conditions-treatments/ex-vivo-lung-perfusion/
Лёгкие (1, )
_ Система лабораторий по биологии, сделай сам. пример создания. (DIY-биология)
Использование исследований на животных для оценки устройств для сохранения органов — руководство для сотрудников промышленности и Управления по контролю за продуктами и лекарствами https://www.fda.gov/media/107701/download (2017)
https://homeostat.krasn.ru/history Уникальная научная установка «Комплекс оборудования для управляемого культивирования изолированных органов» None УНУ. Оборудование разрабатывалась с 60-х годов. см их историю. + диссертация.
— Посмотреть по статье, что за лаборатория.