2_
Изолированные перфузируемые сердца обеспечивают контролируемую среду для имитации заболеваний сердца и оценки терапевтических вмешательств. Путем повторения болезненных состояний и внедрения потенциальных методов лечения этот метод дает ценную информацию о механизмах заболевания и ускоряет разработку новых терапевтических подходов.
Ишемическая болезнь сердца
Модель ишемически-реперфузионного повреждения сердца (ИРИ) ex vivo хорошо известна и широко используется в кардиологических исследованиях на протяжении десятилетий [ 21 ]. В сердцах Лангендорфа ишемию и реперфузию можно вызвать временной перевязкой левой передней нисходящей коронарной артерии при регионарной ишемии или просто остановкой притока перфузии при глобальной ишемии. После установленного эпизода ишемии поток перфузии, насыщенной кислородом, можно возобновить на некоторое время, чтобы имитировать реперфузию. Для оценки ИРИ в сердце можно выполнить сердечную функцию, размер инфаркта, гибель клеток и другие оценки
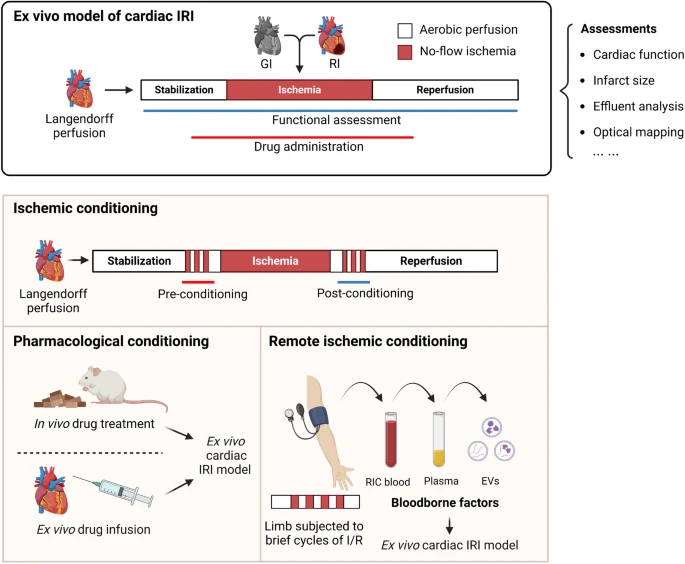
Ex vivo модель сердечной ишемии и реперфузионного повреждения. В изолированных перфузируемых сердцах ишемию можно легко вызвать либо остановкой перфузионного потока, либо временным перевязыванием ПМЖВ. Функциональные и электрофизиологические показатели можно измерять на протяжении всего эксперимента. Кардиопротективные агенты или ингибиторы пути могут вводиться хронически in vivo или в виде острой инфузии ex vivo до, во время и после ишемии. В конце эксперимента можно провести размер инфаркта, анализ компонентов сточных вод, анализ белка и другие анализы. ИРИ, ишемическое и реперфузионное повреждение; GI, глобальная ишемия; RI — региональная ишемия; И/Р – ишемия/реперфузия;
Кардиологические модели IRI ex vivo широко использовались для открытия новых кардиопротекторных агентов или подтверждения кардиопротекторных эффектов существующих препаратов либо путем хронического введения in vivo, либо при острой инфузии ex vivo [ 22 , 23 , 24 , 25 ].
Традиционное применение изолированных перфузированных сердец для изучения аритмии включает проверку анти- и проаритмических эффектов лекарств [ 32 ]. За последние 10 лет развитие оптической электрофизиологии и новых материалов значительно углубило наше понимание электрофизиологии сердца и аритмий, таких как фибрилляция предсердий (ФП) и желудочковая тахикардия (ЖТ).
ФП является наиболее распространенной устойчивой аритмией и наиболее важным фактором риска инсульта [ 33 ]. Долгое время в истории ФП считалась апериодической или случайной. До двадцатого века, с развитием техники оптического картирования, пространственно-временная периодичность наблюдалась при моделировании индуцированной ФП в изолированных перфузированных сердцах [ 34 , 35 ]. Эти исследования предоставили доказательства гипотезы о том, что в предсердиях существуют стабильные, самоподдерживающиеся роторы и что высокочастотная активация такими роторами приводит к сложным паттернам активации, которые характеризуют ФП [ 13 , 36 ]. Однако текущая терапия остается ограниченной, отчасти из-за неспособности картирования одноповерхностных электродов локализовать драйверы ФП в сложном сердце человека. Исследования на перфузированных сердцах человека ex vivo предоставили более глубокое понимание механизмов ФП для определения дальнейшего лечения. Например, Хансен и др. использовали подходы трансмурального оптического картирования высокого разрешения в сочетании с 3D-МРТ с контрастным усилением для определения точных функциональных и структурных особенностей 3D-микроанатомических реентриных драйверов ФП [ 37 , 38 , 39 ].
ЖТ, включая фибрилляцию желудочков (ФЖ), является наиболее распространенной причиной внезапной сердечной смерти [ 40 ]. В изолированных сердцах млекопитающих также наблюдалось, что роторы вносят вклад в механизм ФЖ [ 41 , 42 ]. Это было подтверждено на сердцах человека, перфузируемых по Лангендорфу, в которых роторы и даже волны свитка наблюдались с помощью электрического и трансмурального оптического картирования во время ранней ФЖ [ 43 ]. Генные мутации являются одной из основных причин ФЖ. В изолированных перфузированных сердцах мышей с трансгеном RyR2/RyR2 R4496C или KCNJ2-R67Q при оптическом картировании после индукции адреналина и кофеина наблюдалась повышенная фокальная активность и повторный вход, а также большее количество случаев ЖТ [ 44 , 45 ]. В сердцах, перфузируемых по Лангендорфу, Moreno et al. обнаружили, что влияние острой механической нагрузки и ишемии на частоту и динамику ФЖ ослабевает при сердечной недостаточности по сравнению с нормальным сердцем [ 46 ].