_15_ Мы представляем протокол использования нормотермической системы кровоснабжения ex vivo для доставки терапевтических средств на весь сердечный аллотрансплантат в модели трансплантации гетеротопического сердца свиньи. …. Эффективная доставка к сердцу терапевтических вмешательств, таких как генная, клеточная или иммунотерапия, является существенным препятствием для клинического применения 4 , 5 . Технология, представленная перфузионными устройствами ex vivo, позволяет непрерывно перфузировать трансплантаты, поддерживая их в нерабочем, но метаболически активном состоянии 6 – 9 . Это дает уникальную возможность лечить все сердце с помощью передовых методов лечения, сводя к минимуму потенциальные побочные эффекты системной доставки 10 – 13 . Еще одним преимуществом использования перфузионных устройств ex vivo для терапевтической доставки является то, что они позволяют вводить лекарства в коронарное кровообращение в течение длительных периодов времени, что невозможно при использовании традиционных методов холодного статического хранения. Это позволяет обеспечить более глобальную доставку терапевтических средств к трансплантату 14 . … Используя представленный здесь протокол, мы добились успешной доставки гена люциферазы светлячка в цельный сердечный трансплантат свиньи с использованием аденовирусных векторов 15 . …. На сегодняшний день методы доставки через сердце для этих предполагаемых методов лечения сердечно-сосудистых заболеваний и терминальной сердечной недостаточности основаны на системном введении, внутрикоронарной перфузии посредством катетеризации и прямых внутримиокардиальных инъекциях; все они достигли плохих результатов с точки зрения доставки миокарда 5 , 18 . Ранее мы продемонстрировали надежную и глобальную экспрессию репортерного гена на целых сердечных аллотрансплантатах, когда вирусный вектор вводился в перфузат во время перфузии ex vivo перед трансплантацией 15 . В этом протоколе представлено несколько важных шагов, которые следует подчеркнуть. (1) Необходимо принять все меры предосторожности, чтобы свести к минимуму кровопотерю во время получения сердца от донора. Для перфузионного устройства необходимо получить от донора не менее 1 л крови для достижения адекватной скорости потока. (2) Для терапевтической доставки с использованием нормотермической ex vivo кроветворной перфузии необходимо промыть донорскую кровь перед добавлением ее в перфузат, чтобы удалить любые нейтрализующие компоненты в донорской сыворотке, которые могут отрицательно повлиять на доставку терапевтического препарата к сердцу. (3) Свести к минимуму рассечение сердца донора до момента остановки кардиоплегии, чтобы избежать фатальных аритмий. (4) При введении терапевтического препарата в перфузионное устройство важно вводить его через порт, ближайший к корню аорты, и всегда промывать порт, чтобы обеспечить полную доставку суспензии. Это делается для того, чтобы свести к минимуму любую потенциальную потерю терапевтического препарата в оксигенаторе или трубках внутри контура и гарантировать, что трансплантат получает как можно более высокую терапевтическую концентрацию. (5) Наконец, при выборе места для имплантации трансплантата крайне важно, чтобы это место минимизировало возможность натяжения анастомоза и чтобы не было перекручивания кровеносных сосудов/анастомозов.
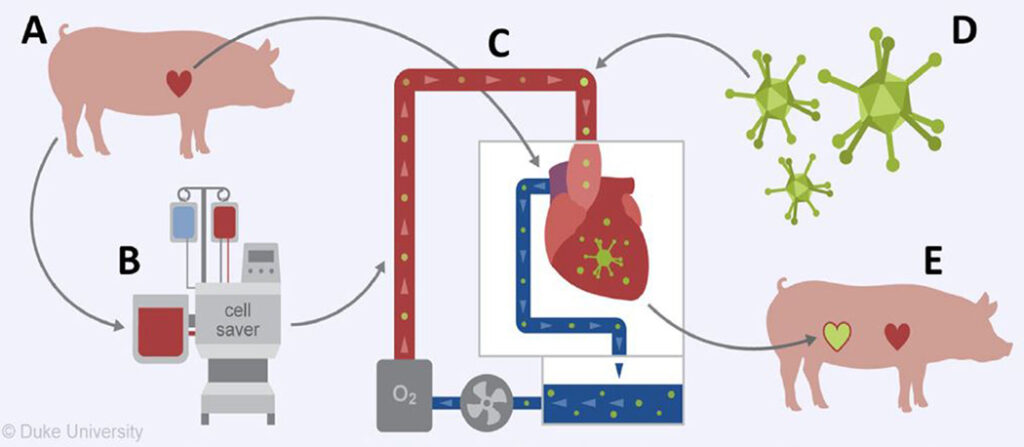
Схема протокола терапевтической доставки всего сердечного аллотрансплантата с использованием нормотермической кроветворной перфузии ex vivo .
( А ) Сердце и кровь берут от свиньи-донора. ( Б ) Кровь промывают с помощью устройства для сохранения клеток для удаления любых терапевтических нейтрализующих компонентов из донорской сыворотки. ( C ) Сердечный аллотрансплантат монтируют на нормотермическое перфузионное устройство ex vivo и перфузируют в течение 2 часов. ( D ) Вскоре после прикрепления аллотрансплантата к перфузату добавляется интересующий терапевтический препарат. ( E ) После отведенного периода перфузии ex vivo аллотрансплантат трансплантируют свинье-реципиенту во внутрибрюшном гетеротопическом положении. Эта цифра была изменена с 15 .